
2025年10月,《Lancet Rheumatol》(《柳叶刀·风湿病学》)刊发了华中科技大学同济医学院附属同济医院风湿免疫科团队的重磅研究——采用普瑞金BCMA CAR-T细胞治疗2例IgG4相关疾病(IgG4-RD)患者,取得了令人振奋的临床效果1。这一突破不仅打破了IgG4-RD复发难治的治疗僵局,更引发了全球风湿免疫领域的广泛关注与学术探讨。
近日,一场围绕“CAR-T治疗IgG4-RD必要性”的跨国学术争鸣在《柳叶刀-风湿病学》杂志上演。法国学者Paul Dalmas团队对这项新兴疗法的“必要性”提出审慎质疑,而来自中国华中科技大学同济医学院附属同济医院的团队则以令人信服的长期随访数据,阐述了抗BCMA CAR-T细胞治疗在满足临床迫切需求中的独特价值2-3。


当传统疗法陷入反复复发与长期用药的循环,CAR-T这种“超级武器”的出现,究竟是过度治疗,还是破局之光?今天,我们从临床需求的视角深入解读。
1. IgG4-RD患者面临的治疗困境:无法回避的“复发循环”
目前,IgG4-RD的治疗核心目标是控制炎症、保护器官功能、预防复发,临床诊疗方案主要围绕传统药物展开,但均存在难以突破的局限性,无法满足部分患者的治疗需求。
首先是糖皮质激素,作为IgG4-RD诱导缓解的一线首选药物,它对疾病发作或复发时的症状控制效果显著,起效迅速,推荐泼尼松30~40 mg/d,逐渐减量维持治疗。但长期使用或反复使用的弊端十分突出:由于缺乏特异性,它会无差别抑制全身免疫系统,可能引发感染风险增加、消化道溃疡、血糖血脂异常、骨质疏松等一系列副作用4。更关键的是,38.5%~50.0%的患者在激素减量后会出现病情进展,复发率居高不下,无法实现长期缓解5-6。
其次是免疫抑制剂与B细胞清除治疗,针对激素耐药或易复发的患者,临床常联合沙利度胺等免疫抑制剂,或采用利妥昔单抗、伊奈利珠单抗等进行B细胞清除治疗。其中,利妥昔单抗作为常用的抗CD20生物制剂,安全性较好,成本也相对可控,对部分患者能起到一定的维持缓解作用4。但这类治疗存在明显短板:利妥昔单抗等药物需要反复给药,且部分患者治疗后仍会出现疾病复发,无法彻底摆脱药物依赖;同时,沙利度胺等免疫抑制剂也存在一定的副作用,长期使用会给患者身体带来额外负担7-8。
此外,对于有明显压迫症状、影响感官功能或面容外形的患者,手术切除可作为系统治疗的辅助方案,但无法从根本上解决免疫异常的核心问题,术后仍存在复发可能。总体而言,现有诊疗方法大多停留在“控制症状”的层面,难以实现“长期无药缓解”,对于多次复发、对多种常规治疗无效的难治性患者,临床需求缺口十分突出。
2. 靶点之争:BCMA靶点可能比CD19靶点更有效
随着细胞免疫治疗技术的发展,CAR-T细胞疗法逐渐进入IgG4-RD治疗领域。目前,针对IgG4-RD的CAR-T治疗主要有CD19和BCMA两个靶点,两者在作用机制、治疗疗效上存在差异。
从作用机制来看,两者的核心差异在于靶向的B细胞群体不同。基础转化研究表明,IgG4-RD受累组织中存在显著的淋巴细胞浸润,B细胞(尤其是记忆B细胞和浆母细胞)是介导疾病发生、发展及复发的关键致病细胞9。
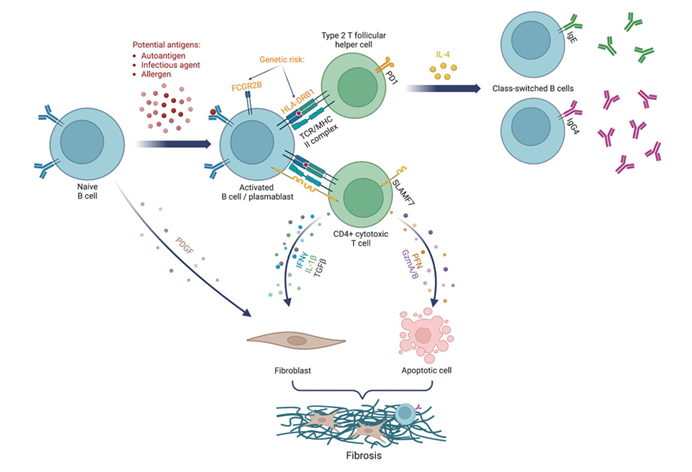
CD19 CAR-T的靶点CD19,表达范围覆盖从原B细胞到记忆B细胞的整个B细胞分化阶段,CD19 CAR-T作用机制是广泛清除体内各类CD19阳性B细胞10。近年来,抗CD19单抗在治疗IgG4-RD已显示出一定疗效,能减少激素用量、降低复发风险。
而BCMA CAR-T的靶点BCMA,表达于B细胞、记忆B细胞及抗体分泌细胞(包括浆母细胞和浆细胞),恰好能广泛靶向IgG4-RD的关键致病细胞亚群。其作用机制是通过CAR-T细胞的特异性识别,高效、精准地清除病变组织中表达BCMA的致病性B细胞,彻底清除致病细胞。这种靶分子表达的区别,正是BCMA CAR-T在IgG4-RD治疗中展现出优异疗效的核心原因。
从临床疗效来看,目前,CD19 CAR-T尚未有明确的治疗IgG4-RD临床病例报道,而华中科技大学同济医学院附属同济医院团队的研究,首次证实了BCMA CAR-T治疗IgG4-RD的显著疗效:2例多次复发、对多种常规治疗无效的患者,接受抗BCMA CAR-T治疗后,投稿时已无药维持缓解达9个月,且未出现任何严重不良事件;后续随访显示,这种无药缓解状态持续超过17个月,这是两位患者既往病程中从未实现过的突破。
3. BCMA CAR-T的临床价值:患者受益风险比
任何治疗方案的临床应用,都需权衡受益与风险,BCMA CAR-T治疗IgG4-RD的核心价值,就在于其为特定患者群体带来的“受益远大于风险”,精准填补了难治性IgG4-RD的临床需求缺口。
首先,从患者受益来看,BCMA CAR-T通过精准清除致病细胞,实现了超过17个月的无药缓解,不仅彻底改善了患者的临床症状,更让患者摆脱了长期用药的负担,显著提升了生活质量——这是传统治疗无法实现的核心受益,也是其最核心的临床价值。
其次,从风险层面来看,BCMA CAR-T的安全性已得到临床验证,且风险可控。Paul Dalmas教授团队曾担忧CAR-T疗法强度大、并发症多(如淋巴细胞清除、感染、细胞因子释放综合征、神经毒性等),但华中科技大学同济医学院附属同济医院的临床研究显示,2例患者接受治疗后,未出现任何严重不良事件,安全性良好。同时,随着CAR-T技术的不断成熟,淋巴细胞清除等潜在风险已能通过规范的临床监测和干预得到有效控制,进一步降低了治疗风险。
更重要的是,BCMA CAR-T的应用并非“替代传统治疗”,而是填补了传统治疗的空白——它主要针对多次复发、对常规治疗无效的难治性患者,这类患者已无更好的治疗选择,BCMA CAR-T为他们提供了一种“救命”的方案。对于病情较轻的患者,传统治疗仍可作为首选。
结语:精准突破,为IgG4-RD治疗开辟新路径
这场围绕BCMA CAR-T治疗IgG4-RD的跨国学术争鸣,本质上是“创新疗法的突破性潜力”与“传统治疗的安全性/经济性”之间的权衡。但不可否认的是,BCMA CAR-T疗法的出现,打破了IgG4-RD难治复发的治疗僵局,精准满足了难治性患者的临床需求。
普瑞金和华中科技大学同济医学院附属同济医院团队的研究,不仅证实了BCMA CAR-T治疗IgG4-RD的显著疗效和安全性,更提示BCMA阳性B细胞可能是介导该病复发的关键致病细胞亚群,为后续研究指明了方向。
正如《柳叶刀》倡导的“最好的科学是为了更好的生活”,BCMA CAR-T疗法的探索与发展,正是医学进步为罕见病患者带来的希望之光。相信在不久的将来,这种精准、高效的治疗方式,将惠及更多IgG4-RD患者,让更多深陷复发困境的患者,实现长期无药缓解,重获健康生活。
参考文献:
1. Cai S, Chen Y, Ye C, et al. Anti-BCMA CAR-T for the treatment of IgG4-related disease: clinical assessment and single-cell transcriptomic analysis. Lancet Rheumatol. 2025 Dec;7(12):e834-e836.
2. Dalmas P, Galicier L, Ebbo M, Schleinitz N. Anti-BCMA CAR T-cell for IgG4-related disease: is this necessary? Lancet Rheumatol. 2026 Feb 18:S2665-9913(26)00039-1.
3. Cai S, Hu Z, Chen Y, Ye C, Zhang J, Sun W, Dong L. Anti-BCMA CAR-T for IgG4-related disease: is this necessary? - Authors' reply. Lancet Rheumatol. 2026 Feb 18:S2665-9913(26)00040-8.
4. 费允云,刘燕鹰,董凌莉,向阳,张文,赵岩.IgG4相关性疾病诊疗规范 [J].中华内科杂志,2023,62(10):1161-1171.DOI:10.3760/cma.j.cn112138-20221105-00830.
5. Yunyun F, Yu C, Panpan Z, Hua C, Di W, Lidan Z, Linyi P, Li W, Qingjun W, Xuan Z, Yan Z, Xiaofeng Z, Fengchun Z, Wen Z. Efficacy of Cyclophosphamide treatment for immunoglobulin G4-related disease with addition of glucocorticoids. Sci Rep. 2017 Jul 21;7(1):6195.
6. Peng L, Nie Y, Zhou J, Wu L, Chen X, Wang F, Li J, Peng Y, Lu H, Zhao L, Li M, Zhao Y, Zeng X, Fei Y, Zhang W. Withdrawal of immunosuppressants and low-dose steroids in patients with stable IgG4-RD (WInS IgG4-RD): an investigator-initiated, multicentre, open-label, randomised controlled trial. Ann Rheum Dis. 2024 Apr 11;83(5):651-660.
7. Liu Y, Jin K, Yang Y, Yang A. Efficacy and safety of rituximab induction therapy and effect of rituximab maintenance for IgG4-related disease: a systematic review and meta-analysis. Eur J Intern Med. 2024 Sep;127:63-73.
8. Yan X, Guo Z, Lyu C, Tang R, Li R, Wang H, Song K, Chen W, He K, Wu D. Renaissance of Phoenix Drug Thalidomide-New Insights into Practical Clinical Application and Optimization Strategies for Managing Adverse Effects in Digestive Diseases. Pharmaceuticals (Basel). 2025 Nov 7;18(11):1689.
9. Perugino CA, Stone JH. IgG4-related disease: an update on pathophysiology and implications for clinical care. Nat Rev Rheumatol. 2020 Dec;16(12):702-714.
10. Taubmann J, Müller F, Yalcin Mutlu M, Völkl S, Aigner M, Bozec A, Mackensen A, Grieshaber-Bouyer R, Schett G. CD19 Chimeric Antigen Receptor T Cell Treatment: Unraveling the Role of B Cells in Systemic Lupus Erythematosus. Arthritis Rheumatol. 2024 Apr;76(4):497-504. doi: 10.1002/art.42784. Epub 2024 Jan 29. Erratum in: Arthritis Rheumatol. 2025 Mar;77(3):365.
11. Hao Q, Sun M, Liu Y. The spectrum of B cells in the pathogenesis, diagnosis and therapeutic applications of immunoglobulin G4-related disease. Clin Transl Immunology. 2023 Nov 28;12(12):e1477.
关于普瑞金
深圳普瑞金生物药业股份有限公司作为国家高新技术企业、广东省细胞与基因治疗创新药物工程技术研究中心、深圳市专精特新企业,其投资方股东涵盖了国家中小企业发展基金、国科嘉和、深圳资本集团、华邦健康(002004)等。多年来,普瑞金深耕于细胞与基因治疗药物领域,其产品管线包含了多个靶点的CAR-T、TCR-T、CAR-NK药物等,适应症广泛,涵盖了血液系统肿瘤、实体瘤和自身免疫疾病等多个治疗领域。普瑞金始终坚持技术平台化、平台产品化、产品商业化、商业国际化的发展策略和道路,是当前业内率先实现CAR-T细胞药物全球多区域授权的领先创新细胞药物企业。
